§ 7. ДИАГРАММЫ СОСТОЯНИЯ
Диаграммы состояния представляют собой графическое изображение фазового состояния сплавов в зависимости от температуры и концентрации компонентов. Диаграммы состояния строят для условий равновесия, т. е. такого состояния сплава, которое достигается при очень малых скоростях охлаждения или длительном нагреве. Диаграммы состояния сплавов в равновесном состоянии являются теоретическими диаграммами, так как истинное равновесие в практических условиях достигается редко. В большинстве случаев сплавы находятся в метастабильном состоянии, т. е. в состоянии с ограниченной устойчивостью.
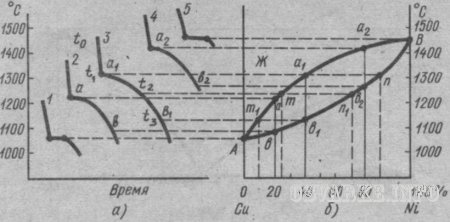
Диаграмма состояния сплавов для случая неограниченной растворимости компонентов в твердом состоянии. Рассмотрим диаграмму состояния сплавов системы медь - никель (рис. 14). Медь и никель, соединяясь в любых пропорциях, образуют непрерывный ряд твердых растворов, так как атомы никеля способны заместить в кристаллической решетке все атомы меди. Температура плавления меди составляет 1083°С, никеля 1445°С.
Рассмотрим кривые охлаждения (рис. 14, а) сплавов системы медь-никель для пяти составов следующей концентрации, %: lOOCu, 80Cu+20Ni, 60Cu+40Ni, 20Cu+80Ni, lOONi. Чистые металлы (кривые 1 и 5) имеют одну критическую точку - температуру затвердевания (кристаллизации), а сплавы (кривые 2, 3, 4) - две, т. е. сплавы в отличие от чистых металлов кристаллизуются в интервале температур. Например, кристаллизация сплава 3 начинается при температуре t1 (точка a1), при этой температуре из жидкого сплава начинают выпадать первые кристаллы твердого α-раствора, а заканчивается кристаллизация при температуре t3 (точка b1). При этой температуре затвердевает последняя капля жидкого сплава. Разная температура конца кристаллизации сплавов свидетельствует о том, что состав твердой фазы непрерывно изменяется.
Для построения диаграммы состояния (рис. 14, 6) на оси абсцисс сетки в координатах температура - концентрация откладывают (отмечают точками) составы пяти сплавов и восстанавливают из каждой точки вертикальные линии. После этого переносят на эти вертикальные линии с кривых охлаждения сплавов критические точки, а на левой и правой ординатах температур отмечают температуры кристаллизации чистых металлов - меди (100%) и никеля (100%). Соединив плавными кривыми температуры начала и конца кристаллизации всех сплавов, получают диаграмму состояния сплавов системы медь-никель с неограниченной растворимостью компонентов в твердом состоянии. Сплавы меди и никеля кристаллизуются и затвердевают в некотором температурном интервале. В пределах этого температурного интервала одновременно существуют две фазы: жидкий сплав и кристаллы твердого раствора - меди и никеля. На диаграмме этот интервал ограничен двумя линиями, соединяющими точки плавления чистых меди и никеля. Верхняя линия обозначает начало затвердевания при охлаждении или конец расплавления при нагреве, нижняя соответственно конец затвердевания или начало плавления. Рассмотренная диаграмма состояния сплава меди и никеля имеет три области. Область существования жидкого расплава лежит выше верхней линии, соединяющей точки плавления меди и никеля, а область существования кристаллических твердых растворов - ниже нижней линии. Между этими линиями находится двухфазная область, в которой одновременно существуют расплав и кристаллы твердого раствора. Верхнюю границу этой области называют линией ликвидус, а нижнюю - солидус («ликвидус» в переводе с латинского означает жидкий, «солидус» - твердый).
По этой же диаграмме состояния можно определить концентрации твердой и жидкой фаз в сплаве при его кристаллизации. Например, для сплава 3 при температуре t2 концентрация фаз определяется горизонтальной линией mn1, проведенной до пересечения с линиями солидус и ликвидус. Точка n1 показывает концентрацию твердой фазы, а точка m - концентрацию жидкой фазы. При температуре t3 концентрация твердой фазы определяется точкой b1 на диаграмме состояния, а концентрация жидкой фазы – точкой m1.
Из сказанного следует, что в процессе кристаллизации непрерывно изменяется состав фаз: жидкой по линии ликвидус и твердой по линии солидус. Кристаллы твердого раствора, выпадающие из жидкого при разной температуре, имеют переменный состав. Выросшие в первый момент кристаллизации, оси кристаллов обычно обогащаются тугоплавким компонентом (никелем), а междуосные пространства заполняются позже и обогащаются более легкоплавким компонентом (медью). Такую неоднородность отдельных кристаллов какого-либо сплава называют внутрикристаллической, или дендритной ликвацией. Дендритная ликвация тем больше, чем больше расстояние между линиями ликвидус и солидус.
Обычно это явление нежелательно и дендритную ликвацию предотвращают последующим длительным нагревом для выравнивания состава сплава, вследствие происходящего в нем диффузионного процесса.
К твердым растворам относят также сплавы систем Си-Аи, Ag-Аи, Ni-Аи, Fe-Cr, Fe-Va, Bi-Sb и др., кристаллизующиеся по рассмотренному типу диаграммы состояния, когда оба компонента неограниченно растворимы в жидком и твердом состояниях и не образуют химических соединений.
Диаграмма состояния сплавов, образующих механические смеси из чистых компонентов. Рассмотрим, например, диаграмму состояния сплавов системы висмут-кадмий (рис. 15). Область существования жидкого расплава ограничена сверху ломаной линией, соединяющей точки плавления висмута и кадмия через точку Е. В точке Е сплав (40% висмута и 60% кадмия) имеет одинаковые температуры ликвидуса и солидуса. Все остальные сплавы системы затвердевают и плавятся в пределах температурного интервала, который снизу ограничен горизонтальной линией солидуса. Сплав в точке Е имеет очень мелкие кристаллы висмута и кадмия, находящиеся в определенном взаимном расположении. Этот сплав называется эвтектикой («эвтектика » в переводе с греческого означает легкоплавкая). Эвтектикой называют механическую смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкого сплава. Твердые сплавы, лежащие левее эвтектической точки Е, и сплавы, содержащие до 40% висмута, называют доэвтектическими, а лежащие правее точки Е и содержащие более 40% висмута - заэвтектическими. Доэвтектические сплавы состоят из смеси кристаллов висмута и эвтектики (кристаллы висмута + кристаллы кадмия), а заэвтектические - из смеси кристаллов кадмия с эвтектикой. По этому типу диаграммы состояния кристаллизуются также сплавы систем Zn-Sn, Pb-Ag, Ni-Cr, Cr-Mn, Cu–Bi, Al-Si.
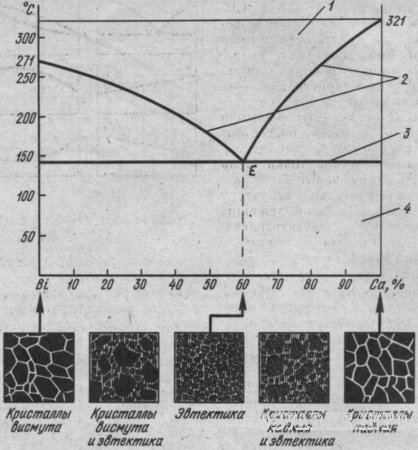
Рис. 15. Диаграмма состояния сплавов висмут-кадмий:
1 – жидкий сплав, 2 – линия ликвидуса, 3 – линия солидуса, 4 – механическая смесь кристаллов висмута и кадмия, Е – эвтектика
Диаграмма состояния сплавов для случая ограниченной растворимости компонентов в твердом состоянии. Одна из таких диаграмм показана на рис. 16, а. Система содержит три фазы - жидкий раствор, твердый раствор компонента В в компоненте А (назовем его α) и твердый раствор компонента А в компоненте В (назовем его β). Линия диаграммы KCD - линия ликвидуса, линия KECFD - линия солидуса. Кристаллы α выделяются из жидкого сплава по линии ликвидуса КС, а кристаллы β - по линии CD. Затвердевание сплавов происходит по линии солидуса КЕ с образованием кристаллов α и по линии DF - с образованием кристаллов β. Одновременная кристаллизация α- и β-фаз с образованием механической смеси кристаллов этих фаз происходит на линии солидуса ECF.
Сплав состава точки С после затвердевания называется эвтектическим, поскольку он состоит только из одной эвтектики α+β. Составы сплавов, лежащих левее эвтектической точки С на линии ЕС после затвердевания, называются доэвтектическими сплавами и имеют структуру α+эвтектика (α+β). Составы сплавов, лежащих правее точки С на линии CF после затвердевания, называются заэвтектическими сплавами и имеют структуру β+эвтектика (α+β).
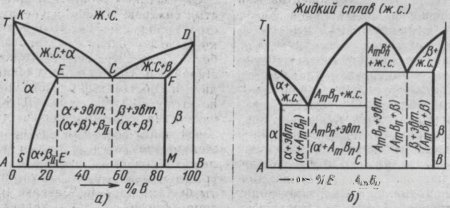
Рис. 16. Диаграмма состояния сплавов для случаев ограниченной растворимости компонентов в твердом состоянии (а) и для случаев образования компонентами А и В химического соединения (б)
Линия ES показывает ограниченную растворимость в твердом состоянии компонента В в компоненте А, уменьшающуюся с понижением температуры. Линия FM показывает растворимость компонента А в В, не изменяющуюся с понижением температуры.
Предельная растворимость компонента В в А характеризуется точкой Е, а А в В - точкой F. При кристаллизации сплавов, состав которых находится левее точки S (или правее точки М), при любой температуре в твердом состоянии все количество компонента В (или А) находится в твердом растворе и структура таких сплавов состоит из зерен α (или β).
В сплавах, состав которых находится между точками S и Е (за пределами растворимости В в А), образовавшиеся при затвердевании кристаллы α при понижении температуры ниже линии ES пересыщены компонентом В и поэтому из них происходит выделение избыточных кристаллов. Этими кристаллами являются кристаллы β концентрации точки М, называемые вторичными (βII). Такие сплавы после полного охлаждения имеют структуру, состоящую из кристаллов α состава точки S и кристаллов βII, т. е. α+βII.
В сплавах состава линии ЕС, имеющих после затвердевания структуру α+эвтектика (α+β), из кристаллов α выделяются кристаллы β и после полного охлаждения структура будет α+эвтектика (α+β)+βII.
Диаграммы состояния сплавов, образующих химические соединения. Сплавы, имеющие химическое соединение (рис. 16, б) компонентов А и В, имеют сложную диаграмму состояния. Химическое соединение обозначают АmВn. Это указывает на то, что в данном соединении на m атомов компонента А приходится n атомов компонента В. Число фаз в данной системе три - жидкий раствор, твердый раствор компонента В в компоненте А (фаза α) и твердый раствор компонента А в компоненте В (фаза β).
Данная диаграмма как бы составлена из диаграмм для двух систем: компонент А – химическое соединение АmВn, и компонент В – химическое соединение АmВn. В сплавах левее точки С компонента А имеется больше, чем входит в химическое соединение АmВn. Следовательно, в этих сплавах левее точки С образуется эвтектика α+АmВn. В сплавах правее точки С компонента В больше, чем может входить в химическое соединение АmВn. Следовательно, в этих сплавах образуется эвтектика АmВn+β.
Связь между свойствами сплавов и типом диаграмм состояния. Между составом и структурой сплава (рис. 17), определяемой типом диаграммы состояния и свойствами сплава, имеется определенная зависимость (правило Н.С. Курнакова). В механических смесях свойства (твердость Н, электропроводность Е и др.) изменяются линейно (рис. 17, а). В твердых растворах свойства изменяются по криволинейной зависимости (рис. 17, 6). В химических соединениях свойства выражаются ломаными линиями (рис. 17, в). При концентрации, соответствующей химическому соединению, отмечается характерный перелом на кривой свойств. Это объясняется тем, что химические соединения обладают индивидуальными свойствами, обычно резко отличающимися от свойств образующих их компонентов.
По диаграммам состояния можно определять и технологические свойства сплавов, что облегчает выбор материала для изготовления изделий. Так, твердые растворы имеют низкие литейные свойства (плохую жидкотекучесть, склонны к образованию пористости и трещин). В свою очередь эвтектические сплавы имеют хорошую жидкотекучесть.
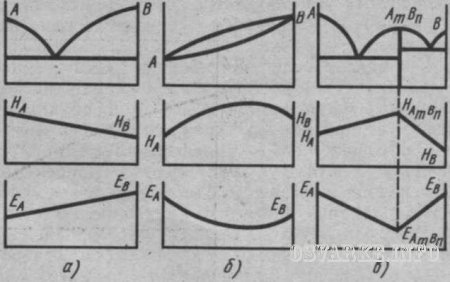
Рис. 17. Диаграмма состав-свойства для сплавов типа:
а - механической смеси, б - твердого раствора, в – химического соединения; А и В компоненты сплава, АmВn - химическое соединение, Н - твердость, Е - электропроводность



Уважаемый посетитель, Вы прочитали статью "Диаграммы состояния", которая опубликована в категории "Материаловедение". Если Вам понравилась или пригодилась эта статья, поделитесь ею, пожалуйста, со своими друзьями и знакомыми.
Наш сайт рекомендует:
26 октября 2011 | Просмотров: 126463 |