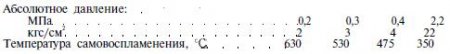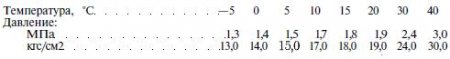Ацетилен представляет собой углеводород ненасыщенного ряда СпН2n-2. Его химическая формула С2Н2, структурная формула Н-С=С-Н. При атмосферном давлении и нормальной температуре ацетилен - бесцветный газ. Технический ацетилен вследствие присутствия в нем примесей, например фосфористого водорода и сероводорода, имеет резкий специфический запах. При 20°С и 760 мм рт. ст. плотность ацетилена р = 1,091 кг/м3. Физические константы ацетилена следующие:
При атмосферном давлении ацетилен сжижается при температуре -82,4...-83,6°С. При температуре -85°С и ниже ацетилен переходит в твердое состояние, образуя кристаллы плотностью 0,76 кг/м3. Жидкий и твердый ацетилен легко взрывается от трения, механического или гидравлического удара и действия детонатора.
Полное сгорание ацетилена происходит по реакции
С2Н2+2,5О2=2СО2+Н2О+Q (1)
Из уравнения реакции (1) следует, что для полного сгорания одного объема ацетилена требуется 2,5 объема кислорода. Высшая теплотворная способность ацетилена при 0°С и 760 мм рт. ст.
равна Qв=58 660 кДж/м3 (14 000 ккал/м3), низшая теплотворная способность при тех же условиях может быть принята Qн=55 890 кДж/м3 (13 500 ккал/м3).
Теплота реакции (1) сгорания ацетилена С} слагается из теплоты реакции экзотермического распада ацетилена и суммы теплот первичных реакций сгорания углерода и водорода. Экзотермический распад ацетилена происходит по реакции
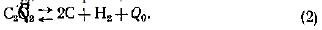
Теплота распада Qо=225,8 кДж/моль (53,9 ккал/г-мол) или Qо=225,8*100/26,036=8686 кДж/кг (2070 ккал/кг).
Теплота сгорания С в СО2 равна 395,7 кДж/моль (94,45 ккал/г-мол), Н2 в Н2О равна 290,4 кДж/моль (68,35 ккал/г-мол). Тогда для теплоты реакции сгорания ацетилена по уравнению (1) получаем 225,8+2-395,7+290,4=1307 кДж/моль (311,15 ккал/г-мол) или Q=1307,6*1000/26,036=50000 кДж, или 50 000*1,17=58 500 кДж/м3 (14 000 ккал/м3);
здесь 1,17 кг/м3 - плотность ацетилена при 0°С и 760 мм рт. ст.
Ацетилен широко используют в химической промышленности в качестве основного исходного вещества для получения ряда важнейших продуктов органического синтеза: синтетического каучука, пластмасс, растворителей, уксусной кислоты и т. п.
Ацетилен - универсальное и самое распространенное горючее, используемое в процессах газопламенной обработки. При сгорании с кислородом он дает пламя с наиболее высокой температурой, равной 3150°С. Достигнуть столь высокой температуры пламени при использовании других горючих не удается.
При использовании ацетилена необходимо учитывать его взрывные свойства, для того чтобы обеспечить полную безопасность работ. Следует всегда иметь в виду, что ацетилен (как и водород) относится к наиболее взрывоопасным газам.
Температура самовоспламенения ацетилена находится в пределах 240-630°С и зависит от давления и присутствия в нем различных веществ:
Повышение давления существенно снижает температуру самовоспламенения ацетилена. Присутствие в ацетилене частиц других веществ увеличивает поверхность контакта и тем понижает температуру самовоспламенения.
Практически в зависимости от давления допустимо нагревание ацетилена до следующих температур: при абсолютном давлении 0,1 МПа (1 кгс/см2) - до 300°С, при абсолютном давлении 0,25 МПа (2,5 кгс/см2) - до 150-180°С, при более высоких давлениях - до 100°С.
Один из важных показателей взрывоопасности горючих газов и паров - величина энергии зажигания. Чем ниже эта величина, тем взрывоопаснее данное вещество. Значения энергии зажигания для газовых смесей стехиометрического состава при атмосферном давлении и 20°С приведены в табл. 1.
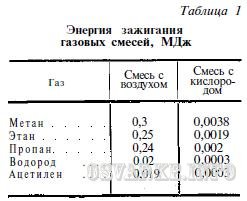
Как видно из этих данных, энергия зажигания кислородно-газовых смесей примерно в 100 раз меньше, чем воздушно-газовых. Ацетилен имеет наименьшую энергию зажигания и в отношении взрывоопасности подобен водороду.
Основной способ получения ацетилена основан на реакции взаимодействия карбида кальция с водой. Карбид кальция СаС2 - твердое вещество кристаллического строения, имеющее в изломе темносерый или коричневый цвет. Плотность химически чистого СаС2 при температуре 18°С равна 2,22 г/см3.
Реакция образования карбида кальция из окиси кальция и углерода является эндотермической и протекает при температуре 1900-2300°С по уравнению
CaO+3C=CaC2+CO-452,5 кДж/моль (108 ккал/г-мол)
56,08+36,03=64,1+28,01. (3)
Согласно уравнению для образования 1 кг СаС2 расходуется 56,08/64,1=0,875 кг СаО и 36,03/64.1=0,562 кг С.
Для получения 1 кг СаС2 требуется теоретически затратить теплоты 452,5*1000/64,1=7060 кДж/кг (1685 ккал/кг).
Технический карбид кальция содержит 70-75% химически чистого СаС2, 17-24% СаО и различные примеси: окислы магния, алюминия, железа, соединения серы, фосфора, ферросилиций, углерод и др.
Карбид кальция чрезвычайно активно вступает во взаимодействие с водой, разлагаясь при этом с образованием газообразного ацетилена и гидрата окиси кальция (гашеной извести). Разложение карбида кальция водой протекает экзотермически: СаС2+2Н2О=С2Н2+Са(ОН)2+127,4 кДж/моль (30,4 ккал/г-мол)
64,1+36,032=26,036+74,096. (4)
Следовательно, для разложения 1 кг химически чистого СаС2 требуется затратить 0,562 кг воды. При этом получается 26,036/64,1=0,406 кг С2Н2 и 74,096/64,1=1,156 кг Са(ОН)2. Плотность ацетилена при 20°С и 760 мм рт. ст. равна 1,09 кг/м3; следовательно, количество ацетилена (выход ацетилена), получаемое пои разложении 1 кг СаС2, равно аm=0,406*103/64,1=372,5 дм3/кг.
С учетом паров, насыщающих ацетилен при 20°С и 760 мм рт. ст. выход ацетилена аm = 380,88 дм3/кг. Количество теплоты, выделяющейся при разложении 1 кг СаС2, 127,4*103/64,1=1980 кДж/кг (475 ккал/кг).
Содержащаяся в качестве примеси в техническом карбиде негашеная известь СаО при взаимодействии с водой также разлагается по реакции СаО+Н2О=Са(ОН)2+63 кДж/моль (15,1 ккал/г-мол) или 63*103/56,08=1130 кДж/кг СаО (270 ккал/кг СаО). (5)
Принимая содержание чистого СаС2 в техническом СаС2 равным 70% и содержание в нем СаО равным 24%, получим тепловой эффект реакции разложения технического карбида кальция: (1980*0,7)/(1130*0,24)=1651 кДж/кг (400 ккал/кг).
Экзотермичность реакции разложения карбида кальция создает опасность перегрева в зоне реакции. В связи с этим необходимо осуществлять ее при избытке воды и обеспечивать отвод теплоты реакции. Особенно опасны местные перегревы карбида кальция, так как при этом температура в месте его разложения может достигать 700-800°С. При такой температуре возможна полимеризация, разложение и взрыв ацетилена, особенно при попадании воздуха в зону реакции. Поэтому необходимо в месте разложения карбида кальция поддерживать
температуру не выше 150°С, при которой еще не могут возникать процессы полимеризации ацетилена. При температуре 200°С и выше может происходить разложение карбида кальция за счет отнятия влаги от гашеной извести по реакции
СаС2+Са(ОН)2-С2Н2+2СаО.
Эта реакция протекает при недостатке влаги, поэтому может произойти сильный перегрев карбида кальция, куски которого будут покрыты плотной коркой гашеной извести. Непрерывное
удаление с кусков карбида кальция слоя образующейся гашеной извести имеет важное значение для полноты разложения карбида кальция и безопасности этого процесса.
Количество ацетилена в литрах (при 20°С и 760 мм рт. ст.), выделяемое при разложении 1 кг карбида кальция, называется выходом ацетилена из карбида кальция. В ГОСТ 1460-56 установлены следующие нормы выхода ацетилена в зависимости от размеров кусков (грануляции) карбида кальция (табл. 2).
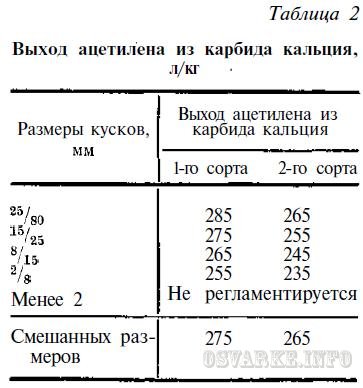
С уменьшением размеров частиц карбида кальция выход ацетилена понижается, что объясняется большим содержанием в мелком карбиде посторонних примесей (СаО и др.).
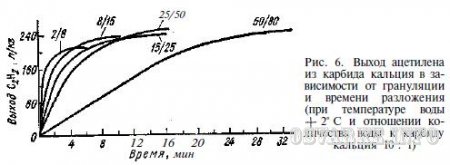
Скорость разложения карбида кальция - важный показатель для его использования в ацетиленовых генераторах - измеряется количеством ацетилена, выделившимся за время разложения 1 кг карбида кальция в течение 1 мин. Скорость разложения (л/кг-мин) зависит от сорта и грануляции карбида кальция, а также от температуры воды. Как видно на рис. 6, наибольшая скорость разложения достигается в первые 2-4 мин после смачивания карбида кальция.
Поскольку карбид кальция жадно поглощает атмосферную влагу и при этом разлагается с выделением ацетилена, его хранят и транспортируют в герметически закрытой таре: барабанах из кровельной стали или контейнерах, герметически закрывающихся крышкой, из листовой низкоуглеродистой стали. Барабаны с карбидом кальция необходимо хранить в сухих, хорошо проветриваемых складах, защищенных от затопления грунтовыми водами.
Способ получения ацетилена из карбида кальция довольно громоздкий, дорогой и требующий затрат большого количества электроэнергии. За последние годы разработаны и быстро внедряются в промышленность более экономичные и высокопроизводительные способы получения ацетилена: из природного газа термоокислительным пиролизом метана в смеси с кислородом (так называемый пиролизный ацетилен) и разложением жидких горючих (нефти, керосина) действием электродугового разряда (так называемый электропиролиз). Получение ацетилена из природного газа на 30-40% дешевле, чем из карбида кальция. Этот ацетилен по своим свойствам не отличается от ацетилена, получаемого из карбида кальция. Пиролизный ацетилен, используемый для сварки и резки, накачивают в баллоны с пористой массой, пропитанной ацетоном.
Хранение и транспортировка ацетилена осуществляются под давлением в баллонах, заполненных специальной пористой массой, пропитанной ацетоном - хорошим растворителем ацетилена, что позволяет существенно увеличить количество ацетилена, накачиваемого в баллон. Кроме того, ацетон снижает взрывоопасность ацетилена. Ацетон удерживается в порах массы и распределяется по всему объему баллона, это увеличивает поверхность его контакта с ацетиленом при растворении и выделении из раствора.
Ацетилен, отпускаемый потребителям в баллонах, называется растворенным ацетиленом (ГОСТ 5457-60). Максимальное давление ацетилена при заполнении баллона составляет 2,5 МПа (25 кгс/см2), при отстое и охлаждении баллона до 20°С оно снижается до 1,9 МПа (19 кгс/см2). При этом давлении в 40-литровый баллон вмещается 5-5,8 кг ацетилена по массе (4,6-5,3 м3 газа при 20°С и 760 мм рт. ст.).
Количество ацетилена в баллоне определяют следующим способом: наполненный баллон взвешивают с точностью до 0,1 кг и выдерживают при температуре не ниже 15°С в течение 8 ч, после чего отбирают ацетилен со скоростью не более 0,8 м3/ч. Остаточное давление в баллоне после отбора должно быть не менее 0,05 МПа (0,5 кгс/см2). После окончания отбора газа баллон вновь взвешивают. Разность между массой наполненного баллона и массой баллона после отбора из него газа представляет собой массу содержавшегося в нем ацетилена.
Давление ацетилена в полностью наполненном баллоне изменяется при изменении температуры следующим образом:
Ацетон (СН3СОСН3) — растворитель, имеющий температуру кипения при атмосферном давлении 56,2°С, температуру замерзания 178,7°К (-94,3°С). При абсолютном давлении 0,1 МПа (1 кгс/см2) и 20°С в 1 кг ацетона растворяется 27,9 кг ацетилена или в 1 л ацетона растворяется 20 л ацетилена. Растворимость ацетилена возрастает в ацетоне примерно прямо пропорционально давлению. С понижением температуры растворимость ацетилена в ацетоне растет.
Для более полного использования емкости баллона порожние ацетиленовые баллоны следует хранить в горизонтальном положении, что способствует равномерному распределению ацетона по всему объему баллона. Наполнять баллоны ацетиленом необходимо медленно (с учетом скорости растворения его в ацетоне) в два приема: сначала в течение 6-9 ч до давления 2,2-2,3 МПа (22-23 кгс/см2), затем после отстаивания вторично до давления 2,3-2,5 МПа (23-25 кгс/см2), так, чтобы после охлаждения до температуры 20°С давление в них составило 1,9 МПа (19 кгс/см2) согласно ГОСТ 5457-60. Для ускорения накачки баллонов иногда их снаружи охлаждают водой, что повышает коэффициент растворимости ацетилена в ацетоне.
При расходовании газа из баллона ацетилен уносит часть ацетона в виде паров. Для уменьшения потерь ацетона отбор ацетилена из баллона следует производить со скоростью не более 1700 дм3/ч, соединяя в случае необходимости несколько баллонов в батарею. По этой же причине нельзя отбирать газ из баллона, в котором давление менее 0,05 МПа (0,5 кгс/см2) при температуре ниже 0°С, менее 0,1 МПа (1 кгс/см2) при температуре 0-15°С, менее 0,2 МПа (2 кгс/см2) при температуре 15-25° С, менее 0,3 МПа (3 кгс/см2) при температуре 25-35°С. Периодически в баллон добавляют ацетон (ацетонируют баллоны) для возмещения потерь растворителя.
При производстве газопламенных работ и децентрализованном потреблении ацетилена растворенный ацетилен имеет ряд существенных преимуществ перед ацетиленом, получаемым из карбида кальция в переносных генераторах непосредственно на месте работ. При использовании ацетиленовых баллонов взамен переносных генераторов производительность труда сварщика повышается на 20%, на 15-25% снижаются потери ацетилена, повышается оперативность и маневренность сварочного поста, удобство работы, безопасность, облегчается использование генераторов в зимнее время. Кроме того, растворенный ацетилен - высококачественное горючее, содержащее минимальные количества посторонних примесей, поэтому его можно применять при выполнении особо ответственных сварочных работ.
Применение растворенного ацетилена в технике газопламенной обработки неуклонно расширяется из года в год, вытесняя использование передвижных ацетиленовых генераторов.
Пористые массы для ацетиленовых баллонов должны удовлетворять следующим требованиям: надежно локализовать взрывной распад ацетилена в баллоне при давлении до 3 МПа (30 кгс/см2); не взаимодействовать с ацетиленом, ацетоном и металлом баллона; обладать достаточной механической прочностью и не разрушаться при толчках и ударах, неизбежных в процессе эксплуатации баллона, не оседать и не образовывать пустот в баллоне; масса должна быть легкой и пористой, чтобы не уменьшать полезного объема и не увеличивать веса тары баллона; не должна выгорать и осмоляться при обратном ударе пламени; должна обеспечивать равномерное распределение ацетона по всему объему баллона и предотвращать
стекание раствора на дно баллона; обеспечивать быстрое выделение ацетилена из раствора для возможности отбора газа без сильного охлаждения баллона.
В качестве пористых масс применяют такие высокопористые вещества, как: инфузорную землю, (кизельгур, диатомит), пемзу, асбест, древесный и активированный уголь, силикат кальция, углекислый магний и др. Наибольшее применение имеют зернистые трамбованные массы и монолитные.



Уважаемый посетитель, Вы прочитали статью "1. Ацетилен, его свойства и получение", которая опубликована в категории "Оборудование и технология". Если Вам понравилась или пригодилась эта статья, поделитесь ею, пожалуйста, со своими друзьями и знакомыми.
Наш сайт рекомендует:
28 апреля 2016 | Просмотров: 19168 |